Algerika
Anwendungshinweise
 Algerika – Das Präparat wirkt krampflösend.
Algerika – Das Präparat wirkt krampflösend.
Darreichungsform und Zusammensetzung
Die Darreichungsform von Algerika ist eine Kapsel: undurchsichtig; auf dem Deckel (Kryształ) befindet sich die schwarze Druckfarbe „TEVA". Im Inneren liegt teilweise zusammengepresstes und granulierter weißer oder fast weißer Wirkstoffpulver. Die Dosierungen sind wie folgt: 25 mg – schwarzer Deckel und hellgelber Körper mit der Aufschrift „7622"; 50 mg – schwarzer Deckel und hellgelber Körper mit radialer schwarzer Linie, Aufschrift „7623"; 75 mg – rosafarbener Deckel, hellgelber Körper mit der Aufschrift „7624"; 150 mg – rosafarbener Deckel und hellgelber Körper mit der Aufschrift „7626"; 300 mg – rosafarbener Deckel, hellgelber Körper mit der Aufschrift „7621". Die Packungsgrößen betragen Blisterpackungen à 7 Stück oder Pappeinheiten mit 2 bzw. 8 Blisterpackungen.
Zusammensetzung: Eine Kapsel.
- Wirkstoff: Pregabalin – in den Dosierungen 25 mg, 50 mg, 75 mg, 150 mg oder 300 mg.
- Hilfsstoffe (bei den Dosierungen 25 mg, 50 mg, 75 mg, 150 mg bzw. 300 mg): Gleitmittel – 9 mg, 18 mg, 8 mg, 16 mg oder 32 mg; Mannitol – 43 mg, 86 mg, 10 mg, 20 mg oder 40 mg; gereinigte Maisstärke – 7 mg, 14 mg, 7 mg, 14 mg oder 28 mg.
Zusammensetzung der Kapselhülle:
- Algerika 25 mg (7622/TEVA): Umfang des Deckels (Nr. 3) wiegt 48 Milligramme; Kapselkörper besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %); Deckel besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %).
- Algerika 50 mg (7623/TEVA): Umfang des Deckels (Nr. 2) wiegt 61 Milligramme; Kapselkörper besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %); Deckel besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %).
- Algerika 75 mg (7624/TEVA): Der Kapselinhalt wiegt 48 Milligramme. Die Kapselhülle besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %). Der Kapseldeckel enthält Titandioxid (2,1747 %), Eisenoxid rot (0,6996 %) und Gelatine (bis zu 100 %).
- Algerika 150 mg (7626/TEVA): Der Kapselinhalt wiegt 61 Milligramme. Die Kapselhülle besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %). Der Kapseldeckel enthält Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %).
- Algerika 300 mg (7621/TEVA): Der Kapselinhalt wiegt 96 Milligramm. Die Kapselhülle besteht aus Titandioxid (2 %), Eisenoxid gelb (0,1 %) und Gelatine (bis zu 100 %). Der Kapseldeckel enthält Titandioxid (2,1747 %), Eisenoxid rot (0,6996 %) und Gelatine (bis zu 100 %).
Zur Beschriftung der Kapseln werden folgende Tinten verwendet: Pharmazeutische Glasur (Lösung von Schellack in Ethanol) – 59,42 %, Isopropanol – 0,55 %, Propylenglykol – 1,3 %, Butanol – 9,75 %, Ethanol – 1,08 %, Eisenoxid schwarz – 24,65 %, Ammoniakwasser – 0,001 % und gereinigtes Wasser – 3,249 %.
Anwendungshinweise
Algerika wird zur Behandlung der folgenden Erkrankungen bei Erwachsenen eingesetzt:
- Fibromyalgie
- neuropathische Schmerzen
- generalisierte Angststörungen
- epilepsie mit partiellen Krampfanfällen, die sich entweder ohne oder mit nachfolgender Generalisierung wiederholen (als Zusatztherapie)
Kontraindikationen
Absolut
- Alter bis zum 18. Lebensjahr
- Schwangerschaft und Stillzeit
- Überempfindlichkeit gegen die Wirkstoffe
Relative Kontraindikationen: Das Präparat sollte bei Vorliegen der folgenden Erkrankungen oder Zustände mit Vorsicht angewendet werden:
- Diabetiker
- Nierenfunktionsstörungen
- Herzinsuffizienz
- Enzephalopathie
- Medikamentenabhängigkeit
- Kombinationstherapie mit Ethanol, Lorazepam und Oxycodon
- Patientenalter von 65 Jahren
Bei Frauen im gebärfähigen Alter ist während der Therapie eine zuverlässige Verhütungsmethode erforderlich.
Anwendung und Dosierung
Die Tabletten werden unabhängig von der Nahrungsaufnahme mit etwas Wasser eingenommen; die Kapseln müssen vollständig geschluckt werden, ohne sie vorher aufzulösen.
Die Tagesdosis liegt zwischen 150 und 600 mg; die Einnahme erfolgt 2- bis 3-mal täglich. Die Therapiedauer wird individuell vom Arzt je nach Befund und den Besonderheiten des Patienten festgelegt.
Die Anfangstagesdosis beträgt bei allen Angaben 150 mg. Eine Erhöhung ist über 3 bis 7 Tage (abhängig von der Therapieantwort und der individuellen Verträglichkeit) zweimal möglich. Ein weiterer Anstieg auf maximal 600 mg ist nach weiteren 7 Tagen ggf. erforderlich.
Die Behandlung wird schrittweise über mindestens sieben Tage abgebrochen.
Bei funktionellen Nierenstörungen wird bei der Dosierungsauswahl die Kreatinin-Klärfunktion (KK) unter Berücksichtigung der entsprechenden Formel beachtet.
- Die Kreatinin-Clearance (Klk) bei Männern berechnet sich nach der Formel: Klk (ml/min) = Körpergewicht (kg) × (140 – Alter in Jahren) / 72 × Serumkreatinin (mg/dl).
- Bei Frauen beträgt die Kreatinin-Clearance (Klk): 0,85 × Klk für Männer.
Die tägliche Dosis Algisk bei hämodialysierten Patientinnen wird unter Berücksichtigung der Nierenfunktion bestimmt; dabei ist unmittelbar nach jeder vierstündigen Dialysesitzung eine zusätzliche Dosis zu verabreichen (ggf. als Tagesdosis oder Anfangsdosis, je nach Häufigkeit der Anwendung).
- Bei einer GFR von 60 ml/min: 150 mg Algisk pro Tag (2–3 Anwendungen).
- Bei einer glomerulären Filtrationsrate (GFR) von 30 bis 60 ml/min: 75 mg Algisk pro Tag (2–3 Anwendungen).
- Bei einer GFR von 15 bis 29 ml/min: 25 bis 50 mg Algisk pro Tag (1–2 Anwendungen).
- Bei einer glomerulären Filtrationsrate (GFR) unter 15 ml/min: 25 mg Algisk einmal täglich.
Die zusätzliche Tagesdosis, die einmalig nach der Dialyse verabreicht wird: Anfangsdosis 25 mg, Tagesdosis 100 mg.
Eine Dosisanpassung für Patientinnen mit Leberfunktionsstörungen ist nicht erforderlich.
Patientinnen ab dem 65. Lebensjahr können aufgrund des altersbedingten Rückgangs der Nierenfunktion Algerika in reduzierten Dosen erhalten.
Die Einzeldosis sollte so rasch wie möglich verabreicht werden; eine Vergrößerung der Dosis ist nicht notwendig.
Nebenwirkungen
Bei der Anwendung von Algerika können folgende Nebenwirkungen beobachtet werden (sehr häufig [≥ 10 %]; häufig [≥ 1 % und < 10 %]; gelegentlich [≥ 0,1 % und < 1 %]; selten [≥ 0,01 % und < 0,1 %]; sehr selten [< 0,01 %, bezogen auf Einzelfälle]):
- Das Nervensystem: sehr häufig – Schläfrigkeit, Schwindel; häufig – Ohnmacht, Beruhigungseffekt, Reizbarkeit, Libidoverlust, Euphorie, Bewusstseinsstörungen, Schlaflosigkeit, Verwirrtheit, Ataxie, Letargie, Tremor, Gedächtnisstörung, Paresthesien, Amnesie; gelegentlich – Halluzinationen, Anorgasmus, Depersonalisation, verstärkte Schlaflosigkeit, Unruhe, Aufregung, Depression, Stimmungsschwankungen, Wortfindungsstörungen, Verlust der Geschmacksempfindungen, unterdrückte Stimmung, Libidozunahme, schreckliche Träume, panische Attacken, kognitive Verwirrungen, Apathie, Hypästhesie, Nystagmus, Myoklonien, Konvulsionen, Abschwächung der Reflexe, Hyperästhesie, Dyskinesie, Brenngefühl auf Schleimhäuten und Haut, psychomotorische Erregung, posturaler Schwindel, Stupor, Intentionstremor, Sprachstörungen, Koordinations- und Gleichgewichtsstörungen sowie Aufmerksamkeitsdefizite; gelegentlich – Parosmie, Hochstimmung, Rastormaschija (Zittern), Hypokinese, Disgrafie;
- Das Verdauungssystem: häufig – Meteorismus, Mundtrockenheit, Erbrechen, Bauchauftreibung und Verstopfung; gelegentlich – Hypästhesie der Mundschleimhaut, gastroösophagealer Reflux sowie vermehrte Speichelabsonderung; gelegentlich – Dysphagie, Ascites und Pankreatitis;
- Das kardiovaskuläre System: selten – AV-Block I. Grades, Hauthyperämie, Palpitationen, arterieller Blutdruckanstieg und Tachykardie; selten – Sinustachykardie, Arrhythmie sowie Bradykardie;
- Das hämatologische System: selten – das Felty-Syndrom, eine Neutropenie sowie eine Thrombozytopenie;
- Infektionen: selten – eine Nasopharyngitis;
- Das urologische System: selten – Harnverhaltung und Dysurie; selten – Oligurie sowie renale Insuffizienz;
- Das respiratorische System: selten – Atemnot, Mundtrockenheit der Nasenschleimhaut; selten – Epistaxis, nasale Obstruktion, Rhinitis, Schluckbeschwerden und Schnarchen;
- Fortpflanzungssystem: häufig – erektile Dysfunktion; selten – retrograde Ejakulation (Hemmung des Samenergusses), vaginale Dyspareunie, Dysmenorrhöe, Mastodynie, Amenorrhoe sowie Sekretion und Hypertrophie der Milchdrüsen;
- Skelett-Muskelsystem: selten – Gelenkergüsse, Muskelzuckungen, Muskelkrämpfe, Muskelverspannungen (Mialgie), Arthralgie, Gliedmaßen- und Rückenschmerzen; selten – Halsbeschwerden, Krampf der Skelettmuskulatur sowie Rhabdomyolyse;
- Haut und subkutanes Gewebe: selten – Pruritus und Papulose; selten – Urtikaria sowie kalter Schweiß;
- Hörorgan und Labyrinthstörungen: häufig – Vertigo; selten – Hyperakusie;
- Sehorgan: häufig – Diplopie, ungenaue Sehwahrnehmung; selten – Gesichtsfeldausfall, Sehstörung, Verminderung der Visusleistung, Augenödem, Augenschmerz, rasche Ermüdung des Sehvermögens (Slesotetschenije), Trockenheit der Augen; selten – Mydriasis, Reizung der Augen, Photopsie ("Funken"), Oszillopsie, Strabismus, Störung der Tiefenwahrnehmung, gesteigerte Lichtempfindlichkeit, Verlust des peripheren Sehvermögens;
- Stoffwechsel und Ernährung: häufig – Gewichtszunahme und Appetitsteigerung; selten – Hypoglykämie, Anorexie, Hyperglykämie; selten – Gewichtsverlust;
- Instrumentelle und laborchemische Befunde: selten – Erhöhung der Kreatinkinase-Aktivität (Kreatinfosfokinase), Aspartataminotransferase sowie Alaninaminotransferase; selten – Hypokaliämie, Hyperkreatininämie;
- Sonstige Symptome: häufig – Schweregefühl, Erschöpfung, Gangstörungen und Ödeme (einschließlich peripherer); selten – Sturz, Asthenie, Durst, generalisierte Ödeme, Herzkompression, Schüttelfrost sowie Schmerzen; selten – Hyperthermie.
Nebenerscheinungen bei der Durchführung der Nachvermarktungsbeobachtung:
- Nervensystem: unbekannter Frequenz – Bewusstseinsverlust, Kopfschmerzen, kognitive Störungen;
- Das Verdauungssystem: selten – Übelkeit, Zungenschwellung, Durchfall;
- Das kardiovaskuläre System: mit unklarer Frequenz – Verlängerung des QT-Intervalls, anhaltende Herzinsuffizienz;
- Das Atemsystem: mit unklarer Frequenz – Lungenödem;
- Das nervöse System: mit unklarer Frequenz – Harnretention;
- Haut und subkutanes Gewebe: selten – Pruritus, Ödeme;
- Sehorgan: bei unklarer Frequenz – Sehverlust;
- Besondere Hinweise:
Allergische Reaktionen: bei unklarer Häufigkeit – Angioödem, Überempfindlichkeit, allergische Reaktion, Stevens-Johnson-Syndrom.
Während der Therapie oder unmittelbar nach Absetzen von Algerika ist die Entwicklung eines epileptischen Status sowie das Auftreten von Grand-Mal-Krämpfen möglich.
Sehstörungen (in Form einer verminderten Sehschärfe bis hin zum Sehverlust) treten in der Regel unabhängig auf, sowohl bei Einstellung als auch bei Fortsetzung der Behandlung.
Es liegen Befunde über die Reversibilität der renalen Insuffizienz nach Absetzen des Algeriks vor.
Nach Abschluss der Behandlung ist das Auftreten eines Syndroms nach dem Absetzen möglich; Frequenz und Schweregrad der Symptome hängen von Dosis und Kurzdauer ab.
Bei Diabetes mellitus kann im Falle einer Gewichtszunahme während der Therapie die Notwendigkeit einer Dosisanpassung der hypoglykämischen Medikamente entstehen.
Im Falle eines Angioödems ist das Präparat sofort abzusetzen.
Während der Einnahme können Schwindel und Somnolenz auftreten, was insbesondere bei älteren Patientinnen das Sturzrisiko erhöht; Vorsicht ist geboten, bis die individuellen Effekte bewertet wurden.
Bei der Behandlung einer Neuropathie können Schmerzen als Hinweis auf eine langdauernde kardiale Insuffizienz bei geriatrischen Patienten mit kardiovaskulären Erkrankungen auftreten.
Das Risiko zentralnervöser Nebenwirkungen (insbesondere Somnolenz) steigt, wenn das Präparat zur Schmerztherapie bei Wirbelsäulenverletzungen eingesetzt wird – ggf. in Kombination mit anderen Medikamenten, einschließlich Spasmolytika.
Bei Auftreten suizidaler Gedanken oder Handlungen muss unverzüglich ein Arzt konsultiert werden.
Patientinnen mit einer Vorgeschichte einer medikamentösen Abhängigkeit sollten das Präparat mit besonderer Vorsicht anwenden.
Als Nebenwirkung wurde eine Enzephalopathie vor allem bei Vorliegen begleitender Zustände beobachtet, die zur Entstehung der Erkrankung prädisponieren.
Bei Bedarf einer kombinierten Anwendung mit opioiden Analgetika sind prophylaktische Maßnahmen gegen Ileus und Obstipation insbesondere bei älteren Patienten erforderlich.
Während der Einnahme von Algofalk ist es notwendig, die Teilnahme an Tätigkeiten mit erhöhter Konzentration und schnellen psychomotorischen Reaktionen zu vermeiden, da dies das Risiko für Nebenwirkungen wie Schwindel, Müdigkeit und Sehstörungen erhöhen kann.
Medikamentöse Interaktionen
Eine pharmakokinetische Interaktion zwischen Algofalk und anderen Substanzen oder Arzneimitteln ist unwahrscheinlich.
Pregabalin verstärkt die motorischen und mnemistischen Funktionsstörungen sowie die Effekte von Lorasepam und Ethanol erheblich.
Bei der kombinierten Anwendung mit opioiden Analgetika kann Algofalk eine Verschlechterung der Funktion des unteren Gastrointestinaltrakts, einschließlich Ileus und Obstipation, hervorrufen.
Lagerungsdauer und Lagerungsbedingungen
An einem für Kinder unzugänglichen Ort bei einer Temperatur von bis zu 25 °C lagern.
Die Haltbarkeitsdauer beträgt zwei Jahre.
Es gibt sehr neugierige medizinische Syndrome; so zum Beispiel das Syndrom des aufdringlichen Saglatywanije (Zwangsgedanken) an Gegenständen. In dem Magen einer Patientin, die an dieser Manie leidet, wurden 2500 fremdartige Gegenstände entdeckt.
Die Überführung des Spenderblutes hat eine fast hundertjährige Geschichte; obwohl dieses Verfahren für viele Menschen völlig gewohnt ist, selbst p...
Abteilung: Artikel über Gesundheit.
Der Mensch wie alle anderen Lebewesen auf unserem Planeten empfinden Wetterveränderungen; es ist normal, meteorologische Schwankungen zu erleben, ohne dass dies gesunden Menschen besondere Beschwerden bereitet. Eine Meteosenstörung ist hingegen ein pathologischer Zustand...
Abteilung: Artikel über Gesundheit.
Gesundheitsverhalten ist heute in Mode, und viele Eltern überlegen, ob das Kind ab dem Kindesalter Sport treiben sollte; doch werden die Trainings ihm helfen, stark und ausdauernd zu werden, die Bewegungskoordination zu verbessern sowie einen positiven Einfluss auf die Psyche zu haben: er wird mehr gesammelt und zielstrebig....
Die Abteilung: Artikel über Gesundheit
Nicht jeder Mensch leidet unter einer Erkältung. Symptome wie Schnupfen und Husten sind jedem bekannt, doch der Berg bleibt einfach...
Die Abteilung: Artikel über Gesundheit
Kaffee ist ein anregendes Getränk, das aufgrund seines belebenden Aromas und des intensiven Geschmacks beliebt ist. Durch seine fördernde Wirkung steigert Kaffee die Arbeitsfähigkeit, unterstützt die Konzentration der Aufmerksamkeit, bekämpft Müdigkeit und verbessert die Stimmung. Laut Statistik leiden daneben 30 % der Bewohner...
Die Abteilung: Artikel über Gesundheit
Es gilt als wissenschaftlich belegte Tatsache, dass eine Ernährung mit hohem Zuckergehalt für die Mehrheit der Bevölkerung attraktiv ist. Dies liegt nicht zwingend an Unmäßigkeit oder mangelnder Disziplin: Die Verbindung des süßen Essens aus dem Säuglingsalter mit dem Gefühl von Ruhe und Sicherheit, das das Kind beim Saugen der Muttermilch empfindet, spielt eine entscheidende Rolle. Zudem verstärkt Zucker im menschlichen Organismus die Wirkung der sogenannten "Glückshormone", auf die wir angewiesen sind. Dennoch findet das Leben selten ohne Süßes statt: Der Verzicht darauf wäre zu groß...
Die Abteilung: Artikel über Gesundheit
Jeder von uns hat mehrfach beobachtet, dass Menschen desselben Geburtsjahres manchmal völlig unterschiedlich sein können.
Die Abteilung: Artikel über Gesundheit
Das Befinden des Menschen hängt von vielen Faktoren ab. Eine der wichtigsten ist die Bewegungsaktivität, die zwar ständig vorhanden, aber nicht zwingend erforderlich ist. Bei verschiedenen Leiden beraten Experten Patienten oft dazu, sich mit Seefahrt zu beschäftigen, was rechtlich als Bewegung gilt.
Die Abteilung: Artikel über die Gesundheit
Sklera und Bindehaut des Auges werden durch Blutgefäße intensiv mit Nährstoffen und Sauerstoff versorgt; im Normalzustand sind diese Gefäße kaum sichtbar, doch bei ihrer Erweiterung färben sich die Skleren rot. Rote Augen deuten oft auf Störungen hin, ausgelöst durch äußere Reize, Allergene oder Erkrankungen.
Die Abteilung: Artikel über die Gesundheit
Gesund und gepflegt auszusehen bedeutet nicht nur, anderen zu gefallen, sondern auch, sich stark, sicher und vital zu fühlen.
Die Abteilung: Artikel über die Gesundheit
Manche meinen, im Medizinwesen des 21. Jahrhunderts gäbe es kaum Geheimnisse mehr; doch das Gegenteil ist der Fall: Je mehr Antworten gefunden werden, desto komplexer stellen sich neue Fragen. Zudem gibt es Erkrankungen, die nicht vollständig erklärbar sind.
Die Abteilung: Artikel über die Gesundheit
Kälte, frische Luft und leichter Schnee verbinden bei vielen Russen mit Munterkeit, Gesundheit und Vergnügen; leider bringt der Winter jedoch auch gesundheitliche Beschwerden mit sich – nicht nur saisonale Erkältungen, sondern oft langdauernde Leiden, deren Symptome vor allem im Winter auftreten.
Die Abteilung: Artikel über die Gesundheit
Wir leben in einer Ära der Werbung: Täglich erhalten Menschen eine Flut aufdringlicher Räte zu Ernährung und Lebensstil.
Abteilung: Artikel über Gesundheit
Zu den wichtigsten chemischen Prozessen im menschlichen Organismus gehören Oxidationsreaktionen, die unter Beteiligung von Fetten und Kohlenhydraten aus der Nahrung sowie Sauerstoff aus der Luft ablaufen. Ein Hauptziel dieser Reaktionen ist...
Abteilung: Artikel über Gesundheit
Die Anwendung pflanzlicher Arzneimittel in der Therapie ist heute aktueller denn je. Präparate aus heilsamen Gräsern können moderne synthetische Medikamente nicht vollständig ersetzen, doch ihre Nutzung wird häufig zur ernsthaften Unterstützung bei der Linderung vieler Leiden und zur Verbesserung der Lebensqualität langjähriger Patientinnen...
Abteilung: Artikel über Gesundheit
Der Arztbesuch ist für viele Menschen kein angenehmes Ereignis, weshalb sie sich oft nicht zu den notwendigen planmäßigen Untersuchungen beeilen. Ein solches Verhalten...
Abteilung: Artikel über Gesundheit
Nach Angaben der Ärzte leiden etwa die Hälfte der Männer im Alter von 25 bis 50 Jahren an Störungen des Prostatabereichs; jedoch wendet sich nur eine Minderheit an einen Arzt. Umsonst – selbst geringes Unwohlsein im Bereich der Geschlechtsorgane kann ein Warnsignal für schwerwiegendere Erkrankungen sein...
Abteilung: Artikel über Gesundheit
In der Medizin werden Infektionen, die vorzugsweise sexuell übertragen werden, heute oft als Geschlechtskrankheiten bezeichnet (früher auch IPPP). Obwohl die Mehrheit dieser Erkrankungen heilbar ist, sind sie weltweit verbreitet, und es besteht keine Tendenz zur Senkung der Morbidität. Wenigen ist bewusst, dass einige Formen bereits im jungen Alter auftreten: Nach Statistiken machen etwa ein Drittel der Männer zwischen 16 und 22 Jahren...
Abteilung: Artikel über Gesundheit
Qualvoller Schnupfen, bei dem jeder Seufzer zum Sieg wird, das Fieber sinkt und das Gelenkreißen nur durch Nachdenken erzwungen wird...
Abteilung: Artikel über Gesundheit
Wenn der Nahrungstrieb überwunden ist und die Möglichkeit fehlt, vollwertig zu essen, treten Perekussys auf – kleine Portionen nach dem Umfang, die den Blutzuckerspiegel stabilisieren helfen. Die Beziehung von Diätassistenten zu Perekussys ist oft negativ, aber nur wegen des Katsch...
Abteilung: Artikel über Gesundheit
Mögen Sie allen singen? Kleine Kinder beschäftigen sich gerne mit Gesang und denken nicht besonders über das Treffen in die Melodie nach. Erwachsene schämen sich meist und fürchten, ihre Talente auf diesem Gebiet vorzuführen, doch dies ist vergeblich: Gesang ist sehr gesundheitsfördernd...
Abteilung: Artikel über Gesundheit
Der Zustand der Wirbelsäule im menschlichen Organismus beeinflusst zahlreiche Funktionen; die Wirbelsäule dient nicht nur als Stütze für den Körper, sondern erfüllt auch weitere Aufgaben...
Abteilung: Artikel über Gesundheit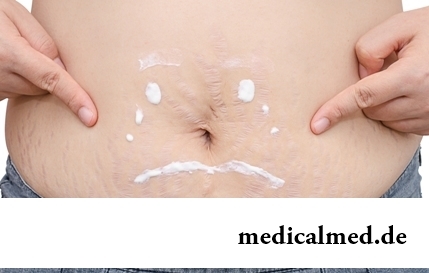
Striae distensae (Dehnungsstreifen) sind Hautdefekte in Form gerader oder welliger Streifen mit einer Länge von 1 bis 10 cm und einer Breite von 1–5 mm. Meistens treten bei Frauen Dehnungsstreifen am Bauch, an den Hüften, auf der Brust sowie an den Gesäßbacken auf. Bei Sportlern können sie zudem an Schultern und Waden vorkommen...
Fachabteilung: Artikel zur Gesundheit
Hämorrhoiden sind eine außerordentlich häufige Erkrankung. Die periodisch auftretenden Entzündungen und Blutungen verursachen bei fast 15 % der Erwachsenen ein ernstes Unwohlsein. Kennt man die Ursachen für das Fortschreiten des Leidens und handelt entsprechend, so kann man den Grad der unangenehmen Empfindungen erheblich verringern sowie das Fortschreiten der Erkrankung verlangsamen.
Fachabteilung: Artikel zur Gesundheit
Während eines Fußspaziergangs wird das Blut in Organe mit florider Durchblutung geleitet; alle Organe werden damit mit einer großen Menge an Sauerstoff versorgt.
Fachabteilung: Diashow
Kosmetika zur Verbesserung von Hautzustand, Nagel- und Haarqualität werden von jeder Frau verwendet. Die Kosten für die regelmäßige Anschaffung modischer Produkte bekannter Hersteller sind für viele sehr hoch und stellen ein erhebliches Problem dar.
Fachabteilung: Artikel zur Gesundheit
Das Klimakterium ist der Prozess des Erlöschens der Fortpflanzungsfunktion des Organismus im Laufe des Alterns. Ein Hauptmerkmal des Eintritts bei Frauen ist die Unterbrechung des Menstruationszyklus. Offiziell wird eine Menopause diagnostiziert, wenn über 12 Monate keine Menstruationen beobachtet werden. Die altersbedingten Veränderungen werden häufig von emotionalen Störungen, einer gestörten Temperaturregulation und vermehrtem Schwitzen, Schwindelanfällen sowie Kopfschmerzen, Tachykardie und anderen unangenehmen Symptomen begleitet. Dieser Komplex der Symptome...
Fachabteilung: Artikel zur Gesundheit