Äquivalenz von Karboplatin
Anwendungshinweise
 Karboplatin-Äquivalenz
Karboplatin-Äquivalenz
Darreichungsform und Inhalt
Die Äquivalenzwerte von Karboplatin werden als Konzentrat zur Herstellung von Infusionslösungen geliefert: durchsichtig, farblos oder nahezu farblos (in braunen Glasflaschen in den Größen 5, 15, 45, 60 oder 100 ml; jede Flasche befindet sich in einer Pappschachtel).
Die Zusammensetzung des Konzentrats zur Herstellung von Infusionslösungen beträgt pro 1 ml:
- Wirkstoff: Karboplatin – 10 mg;
- Hilfsstoffe: Natriumhydroxid, wasserfreies Natriumphosphat und Wasser für Injektionszwecke.
Anwendungshinweise
- Hilfsstoffe: Natriumhydroxid, wasserfreies Disodiumphosphat und Wasser für Injektionszwecke.
- Anwendungshinweise
- Gebärmutterhalskarzinom
- Lungenkarzinom
- Harnblasenkarzinom
- Kopf-Hals-Tumore
Kontraindikationen
- Nachgewiesene Nierenfunktionsstörung (bei einer Kreatinin-Clearing-Rate ≤ 15 ml/min)
- Hämatopoese-Störung
- Schwangerschaft und Stillzeit
- Überempfindlichkeit gegen die Wirkstoffe des Präparats sowie andere Platinverbindungen
- Überempfindlichkeit gegenüber den Komponenten des Präparats sowie anderen Platinverbindungen
Anwendungsweg und Dosierung
Karboplatin kann als Monotherapie oder gleichzeitig mit anderen zytostatischen Arzneimitteln angewendet werden. Das Dosierungsregime wird individuell vom Arzt festgelegt. Das Präparat wird intravenös in den folgenden Dosierungsregimen appliziert:
- 300–400 mg/m² werden über 15 bis 60 Minuten oder als 24-stündige Infusion intravenös appliziert;
- 100 mg/m² werden täglich über 15 bis 60 Minuten im Verlauf von 5 Tagen intravenös appliziert.
Die Gabe des Präparats wird in Abständen von mindestens vier Wochen wiederholt, sofern die Neutrophilen nicht unter 2000/mm³ und die Blutplättchen nicht unter 100.000/mm³ liegen.
Die therapeutische Dosis von Karboplatin kann je nach Nierenfunktion oder Zustand des Knochenmarks wie folgt angepasst werden:
- Patientinnen mit Risikofaktoren (z. B. nach einer myelosuppressiven Therapie oder bei niedrigem funktionellem Status): Die Ausgangsdosis ist um 20–25 % zu verringern.
- Patientinnen mit Nierenfunktionsstörungen (bei einer Kreatinin-Klärfunktion von weniger als 60 ml/min): Aufgrund des erhöhten Risikos für eine schwere Myelosuppression muss die Dosis des Präparats angepasst werden (bei einer Kreatinin-Klärfunktion von 41–59 ml/min auf bis zu 250 mg/m², bei einer Kreatinin-Klärfunktion von 16–40 ml/min auf bis zu 200 mg/m²).
- Patientinnen mit Symptomen einer schweren oder mäßigen hämatologischen Toxizität (bei einer Thrombozytenzahl von <50.000/µl und einem Neutrophilen-Wert von <500/µl): Eine Dosisreduktion auf 25 % kann gefordert werden (sowohl bei Monotherapie als auch im kombinierten Behandlungsschema).
- Patientinnen, die älter als 65 Jahre sind: Es ist eine Anpassung der Anfangs- und der nachfolgenden Dosen möglich.
Diese Empfehlungen basieren auf dem Dosierungsregime und orientieren sich an der Ausgangstherapie; im Folgenden müssen die Dosen je nach Verträglichkeit von Karboplatin sowie dem Verlauf der Myelosuppression angepasst werden.
Die Ausgangsdosis des Präparates in Milligramm wird mittels der Calvert-Formel bestimmt, welche die Abhängigkeit vom Wert der glomerulären Filtrationsrate (GFR in ml/min) und der gewünschten Konzentration von Karboplatin-AUC (AUC in mg/ml × min) beschreibt.
Die Gesamtdosis (in Milligramm) wird nach der Calvert-Formel berechnet, wobei sie von der glomerulären Filtrationsrate (GFR in ml/min) und dem gewünschten AUC-Wert abhängt.
Der angestrebte Wert für die AUC:
- 5–7 mg/(ml·min): bei der Durchführung einer Monotherapie bei zuvor unbehandelten Patienten;
- 4–6 mg/(ml·min): bei der Durchführung einer Monotherapie bei früher behandelten Patienten oder bei der Kombinationstherapie (mit Cyclophosphamid) bei zuvor unbehandelten Patientinnen.
Vor der Applikation von Karboplatin ist eine Verdünnung auf eine Konzentration von maximal 0,5 mg/ml erforderlich; dies kann entweder mit 0,9 %iger Natriumchlorid-Lösung oder 5 %iger Dextrose-Lösung erfolgen.
Die verdünnte Lösung des Präparates behält ihre Stabilität für bis zu 8 Stunden bei Raumtemperatur (25 °C) und für bis zu 24 Stunden bei Lagerung im Kühlschrank (4 °C).
Nebenwirkungen
Bei der Anwendung von Karboplatin können folgende unerwünschte Wirkungen auftreten:
- Hämatopoetische Organe: Der toxische Faktor, der die Dosis von Karboplatin maßgeblich begrenzt, ist die Unterdrückung der Funktion des hämatopoetischen Systems. Die Myelosuppression weist einen dosisabhängigen Verlauf auf. In der Regel wird ein niedriger Spiegel an Blutplättchen und Granulozyten bis zu 2–3 Wochen nach dem Datum des Beginns der Karboplatin-Therapie erreicht; dabei tritt eine Thrombozytopenie häufiger auf. Die Erholung dauert gewöhnlich mindestens vier Wochen, um den Spiegel zu erreichen, der für die Verabreichung der nächsten Dosis notwendig ist. Bei einer ausreichenden Anzahl von Patientinnen können auch Zeichen einer Anämie (Hämoglobin-Spiegel unter 11 g/dl) beobachtet werden. Ihre Intensität hängt von der kumulativen Dosis ab. In einigen Fällen kann eine Transfusionstherapie erforderlich sein, insbesondere bei Patientinnen, die das Präparat langdauernd verwenden (zum Beispiel über mehrere 6-Zyklus-Phasen). Zudem besteht die Wahrscheinlichkeit für klinische Komplikationen wie Infektionen, Fieber, Blutungen sowie septischen Schock oder Sepsis.
- Gastrointestinaltrakt: In den ersten 6–12 Stunden nach der Verabreichung von Karboplatin kann das Risiko des Auftretens von Erbrechen und/oder Übelkeit (von leicht bis mäßig) bestehen, die bis zu 24 Stunden oder länger andauern kann. Das Risiko eines Brechereignisses lässt sich durch die Anwendung antiemetischer Mittel, durch eine ununterbrochene intravenöse Infusion von Karboplatin über 24 Stunden oder durch die Aufteilung der verordneten Dosis auf mehrere Tage nacheinander verringern. In einigen Fällen können zudem auftreten: Diarrhöe, Schleimhautentzündung des Mundes, abdominale Schmerzen und Verstopfung.
- Zentrales und peripheres Nervensystem: Es besteht das Risiko einer peripheren Neuropathie, die sich vor allem durch Paresthesien und eine Absenkung der tiefen Sehnenreflexe manifestiert (insbesondere bei Patientinnen über 65 Jahren mit langwieriger oder vorausgehender Cisplatin-Therapie). Auch Funktionsstörungen des Zentralnervensystems sind möglich. Die Langzeitanwendung des Präparats kann zu einer kumulativen Neurotoxizität führen.
- Organ des Gehörs: Otototoxizität (Geräuschwahrnehmung in den Ohren und Hörverlust).
- Sehkraft: Es besteht das Risiko einer vorübergehenden Verschlechterung oder eines vollständigen Verlustes der Sehkraft (möglicherweise Verlust der Fähigkeit, Licht zu sehen und Farben zu unterscheiden), sowie anderer Funktionsstörungen des Sehapparats. In der Regel erfolgt die vollständige Wiederherstellung und/oder Verbesserung der Sehkraft im Laufe einiger Wochen nach Beendigung der Therapie. Bei Patientinnen mit vorbestehenden Niereninsuffizienzen kann sich eine kortikale Blindheit entwickeln.
- Nieren: Das Auftreten einer leichten und vorübergehenden Erhöhung der Harnstoff- und Kreatinin-Werte im Blutserum ist möglich. Schwere Nierenschädigungen werden in seltenen Fällen beobachtet. Das Risiko für die Entwicklung einer Nephrotoxizität unter Anwendung von Karboplatin (Senkung der Klärfunktion des Kreatinins) steigt bei Erhöhung der Dosis sowie bei Patientinnen, die zuvor eine Cisplatin-Therapie erhalten haben.
- Leber: Eine leichte und in der Regel kurzzeitige Erhöhung der Konzentrationen von Aspartat-Aminotransferase, alkalischer Phosphatase und Bilirubin im Blutserum ist möglich. Bedeutende Funktionsstörungen der Leber können bei Patientinnen auftreten, die hohe Dosen des Präparats mit autologer Knochenmarktransplantation erhalten haben.
- Elektrolytgleichgewicht: Hypokaliämie, Hypomagnesiämie und/oder Hyponatriämie sind möglich.
- Allergische Reaktionen: Fieber, erythematöse Ausschläge, Juckreiz, Bronchospasmus, Urtikaria, anaphylaktische Reaktionen sowie arterielle Hypotension. Diese Reaktionen können bereits wenige Minuten nach der Verabreichung des Präparats beobachtet werden. In seltenen Fällen kann sich eine exfoliative Dermatitis entwickeln;
- Sonstige: Alopecia, Geschmacksveränderungen, Asthenie, grippeähnliche Symptome (Fieber, Temperaturerhöhung), hämolytisch-urämisches Syndrom, Arthralgie/Myalgie, zerebrovaskuläre Störungen sowie allergische Reaktionen direkt an der Injektionsstelle.
Besondere Hinweise
Die Gabe von Karboplatin sollte ausschließlich einem erfahrenen Arzt vorbehalten bleiben, der über Expertise in der Anwendung zytotoxischer Medikamente verfügt. Während der Therapie ist eine kontinuierliche Überwachung der Entwicklung möglicher toxischer Effekte erforderlich, insbesondere bei hohen Dosierungen.
Männer und Frauen müssen während der Anwendung von Karboplatin zuverlässige Kontrazeptionsmaßnahmen anwenden.
Für die Zubereitung und Applikation der Lösung dürfen Spritzen, Nadeln, Infusionssysteme sowie Katheter nicht verwendet werden, die Aluminium enthalten, da das Metall mit dem Wirkstoff reagieren kann und so zu Aktivitätsverlust oder Ablagerungsbildung führt.
Einmal wöchentlich sind periphere Blutparameter sowie Kennzahlen der Leber- und Nierenfunktion (kontrolliert über die renale Klärfunktion mittels Kreatinin) zu überwachen.
Zusätzlich ist es empfehlenswert, neurologische Untersuchungen regelmäßig durchzuführen; dies gilt insbesondere für Patienten ab 65 Jahren sowie für Patientinnen im höheren Alter mit einer früheren Cisplatin-Therapie.
Da Karboplatin kumulative otootoxische Effekte hervorrufen kann, sollten Patienten audiologische Untersuchungen bis zum Beginn und während der Therapie durchführen. Bei klinisch bedeutsamen Störungen der Hörfunktion ist eine Therapieunterbrechung oder eine Dosisanpassung des Präparats erforderlich.
Während der Therapie sind alle üblichen Vorsichtsmaßnahmen zu beachten, die für die Anwendung zytotoxischer Medikamente gelten.
Da Karboplatin kumulative otootoxische Effekte hervorrufen kann, sollten Patienten audiologische Untersuchungen bis zum Beginn und während der Therapie durchführen. Bei klinisch bedeutsamen Störungen der Hörfunktion ist eine Therapieunterbrechung oder eine Dosisanpassung des Präparats erforderlich.
Während der Therapie sind alle üblichen Vorsichtsmaßnahmen zu beachten, die für die Anwendung zytotoxischer Medikamente gelten.
- Die gleichzeitige Anwendung anderer myelosuppressiver Arzneimittel oder die Strahlentherapie kann das Risiko für hämatologische Toxizitäten erhöhen.
- Die gleichzeitige Gabe von Aminoglykosiden und anderen nephrotoxischen Arzneimitteln kann das Auftreten oto- bzw. nephrotoxischer Effekte verstärken.
Lagerungsdauer und -bedingungen
An einem für Kinder unzugänglichen Ort bei Lichtschutz und einer Temperatur von bis zu 25 °C lagern.
Die Haltbarkeitsdauer beträgt drei Jahre.
Bei regelmäßigem Solarium-Besuch steigt das Risiko für Hautkrebs auf 60 %.

Ein unangenehmer Geschmack im Mund kann auf mangelnde morgendliche Hygiene oder die Aufnahme bestimmter Nahrungsmittel zurückzuführen sein.
Rubrik: Artikel zur Gesundheit.
Eine Phobie ist eine wider den Willen des Menschen auftretende, spezifische Angst vor einem bestimmten Inhalt. Während die Angst eine physische Abwehrfunktion der Psyche darstellt, stellt die Phobie deren Abweichung.
Rubrik: Artikel zur Gesundheit.
Hersteller von Milchersatz für Kinder versichern, dass diese Produkte ideal auf die Bedürfnisse von Säuglingen abgestimmt sind. Ist eine Mutter gezwungen, ein Kind infolge schwerwiegender Gesundheitsprobleme künstlich zu ernähren, so ist der Ersatz der Muttermilch notwendig. Kinderärzte bemerken jedoch, dass Frauen häufig ohne schwerwiegende Gründe vom Stillen abweichen und auf die Verwendung von Milchersatzprodukten umsteigen; verbreitete Motive für diese Entscheidung sind das Streben nach schneller Mobilität.
Rubrik: Artikel zur Gesundheit.
Unangenehme Zustände wie die sogenannte Milchfrau (Stillbeschwerden) können fast jeder Frau im Laufe ihres Lebens widerfahren.
Rubrik: Artikel zur Gesundheit.
Ein kurz nach der Geburt befindliches Kind ist von der Liebe seiner erwachsenen Familienmitglieder sowie ihren Sorgen umgeben; ohne diese Unterstützung kann ein Kleinkind nicht existieren. Manche Eltern meinen fälschlicherweise, dass zarte Zuneigung und Liebkosungen völlig ausreichen, damit sich das Kind richtig entwickelt und glücklich wird.
Abteilung: Artikel zur Gesundheit
Der menschliche Körper besteht zu etwa 60 % aus Wasser. Dieser Anteil ist für das normale Funktionieren des Organismus so entscheidend, dass bereits ein Flüssigkeitsverlust von anderthalb Prozent unangenehme Folgen nach sich zieht. Solche Probleme können auch den gesündesten Menschen ereilen, wenn sie beispielsweise einige Stunden in der prallen Sonne verbringen und kein Getränk dabei haben; in diesem Fall lässt sich das Befinden jedoch sehr einfach korrigieren. Viel komplizierter gestaltet sich hingegen die Minimierung der Folgen anderer Ursachen...
Abteilung: Artikel zur Gesundheit
Hohes Fieber ist ein häufiges Symptom weit verbreiteter Erkrankungen wie Infekten (ORVI), Angina pectoris oder Pneumonie, um diese Hitze zu senken...
Abteilung: Artikel zur Gesundheit
Zucker ist ein raffiniertes Produkt, das für den Organismus des modernen Menschen keinen besonderen Wert hat. Der Zuckerkonsum in der Nahrung basiert vor allem auf einer psychologischen Abhängigkeit, die durch den Wunsch nach Süßem ausgelöst wird und sich daraus weiterentwickelt...
Abteilung: Artikel zur Gesundheit
Gelehrte strebten stets danach, grundlegende Erklärungen für medizinische Probleme zu finden. Ihre Theorien bildeten die Basis für moderne Behandlungsmethoden schwerster Pathologien und halfen, unzählige Leben zu retten. Jedoch sind auch solche theoretischen Konstruktionen bekannt, deren Folgen der Menschheit Not und Qual gebracht haben und das Schicksal sowie die Gesundheit vieler Menschen verdorben haben...
Abteilung: Artikel zur Gesundheit
Die Lebenserwartung variiert je nach Region weltweit und wird maßgeblich von Faktoren wie sozialer Stabilität sowie ökonomischen Rahmenbedingungen beeinflusst.
Abteilung: Artikel über Gesundheit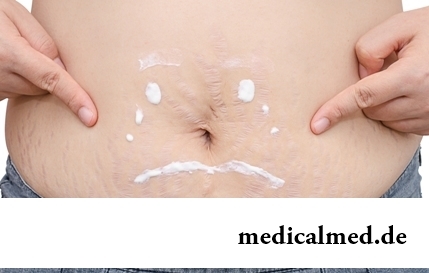
Striae (Dehnungsstreifen): geradlinige oder wellenförmige Hautdefekte mit einer Länge von 1 bis 10 cm und einer Breite von 1–5 mm. Bei Frauen treten sie typischerweise am Bauch, an den Hüften, auf der Brust sowie an den Gesäßbacken auf; bei Sportlern können sie zudem an Schultern und Oberschenkeln entstehen.
Abteilung: Artikel über Gesundheit
Bierliebhaber in unserem Land sind zahlreich. Nach Statistiken konsumiert jeder durchschnittliche Russe (einschließlich Frauen und Kinder) jährlich etwa 60 Liter dieses Getränks. Dies ist weniger als in Tschechien oder Deutschland, doch die Zahl bleibt dennoch beeindruckend. Es gibt nichts zu feiern: Trotz Versicherungen der Produzenten, dass Bier absolut unschädlich sei, darf man die Folgen eines floriden Konsums keinesfalls positiv bewerten. Der Bereich negativer Wirkungen, der populär ist...
Abteilung: Artikel über Gesundheit
Die Zuckerkrankheit des zweiten Typs hat sich in den letzten Jahrzehnten zu einem weltweiten Problem entwickelt. Die Anzahl der Erkrankungsfälle steigt jährlich...
Abteilung: Artikel über Gesundheit
Herpes simplex Typ 1 (eine Infektionskrankheit, die sich durch periodische Pusteln auf den Lippen äußert) zählt zu den am weitesten verbreiteten Leiden. Nach Statistiken sind etwa 50 % der Bevölkerung empfänglich für diesen Erreger, und...
Abteilung: Artikel über Gesundheit
Zellschichtzellulitis (Cellulite): ein sehr häufiger kosmetischer Mangel, der bei Frauen früh oder in bis zu 80 % der Fälle spät auftritt. Sein Auftreten ist mit dem Strukturwandel des subkutanen Fettgewebes verbunden. Zunächst zeigt sich an der Hautoberfläche Unebenheit (Rundungen und Einbuchtungen), gefolgt von kleinen Verdichtungen, was den sogenannten „Apfelhaut-Effekt" darstellt. Die Veränderungen im Zustand des subkutanen Gewebes deuten auf eine hormonelle Dysbalance im Organismus hin.
Die Abteilung: Artikel über Gesundheit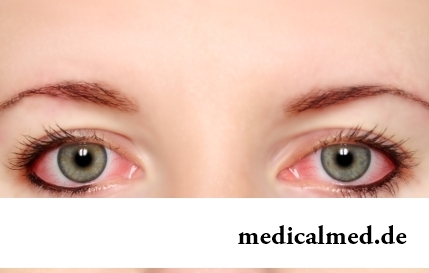
Sklera und die Augenschleimhaut werden intensiv mit Blutgefäßen versorgt, um das Nervengewebe des Organs zu sättigen.
Die Abteilung: Artikel über Gesundheit
Bis vor kurzem schien die Perspektive von Herzerkrankungen für die Mehrheit der Menschen fern und nebelig. Doch früh oder spät stößt jeder erwachsene Mensch auf äußerst unangenehme Empfindungen, wie den schlagartigen Schmerz in der Brust. Sich zu diesem Zeitpunkt durch Gedanken an T zu trösten...
Die Abteilung: Artikel über Gesundheit
Die sprichwörtliche Redewendung 'satt hungrig' ist hier nicht gemeint. Im weitesten Sinne geht es darum, dass wir Menschen oft die Besonderheiten von Zuständen nicht verstehen können, wenn diese uns unbekannt sind. Wenn physiologische Merkmale eines Patienten klarer verlaufen (der Patient spürt, ihm wird schlecht), so ist das Verhalten bei Symptomen, die den psychischen Bereich betreffen, deutlich komplizierter. Es wird nicht nur ein ungewöhnliches Verhalten wie lächerliche Abergläubigkeit angenommen, sondern häufiger wahrgenommen...
Die Abteilung: Artikel über Gesundheit
Bei jedem Menschen tritt gelegentlich leichtes Unwohlsein auf, das er 'auf den Beinen' verdrängt, indem er sich bemüht, keine ärztliche Inanspruchnahme vorzunehmen. Argu...
Die Abteilung: Artikel über Gesundheit
Das Klimakterium oder die Menopause ist ein physiologischer Prozess der Unterbrechung der reproduktiven Funktionen bei Frauen, begleitet von signifikanten hormonellen Veränderungen im Organismus. Die Menopause beginnt in der Regel zwischen dem 50. und 55. Lebensjahr; jedoch sind die Merkmale dieses Prozesses stark individuell unterschiedlich.
Abteilung: Gesundheitsartikel
Ein vollständiger Hörverlust verschlechtert die Lebensqualität erheblich. Verkehrsschwierigkeiten führen zu Einsamkeit und Rückzug. Menschen mit schwerem Hörverlust sehen sich in ihrer sozialen und beruflichen Realisierung behindert und haben im Privatleben häufig Probleme.
Abteilung: Gesundheitsartikel
Die Assel – eine unscheinbare, anspruchslose Pflanze, die auf dem gesamten Gebiet unseres Landes vorkommt. Sie wächst schnell und manchmal unkontrolliert...
Abteilung: Gesundheitsartikel
Für die Bewohner der südostasiatischen Länder sind die vielfältigen Meerespflanzen ein wesentlicher Bestandteil der täglichen Ration. Ihre Popularität beruht nicht nur auf dem hohen Genusswert, sondern auch auf zahlreichen gesundheitsfördernden Eigenschaften. Die Russen sind damit wenig vertraut...
Abteilung: Gesundheitsartikel
Jod ist eines der wichtigsten Spurenelemente im menschlichen Körper. Seine Hauptfunktion besteht in der Synthese der Schilddrüsenhormone, die für einen Großteil der Stoffwechselprozesse verantwortlich sind. Diese Hormone bestehen zu über 65 % aus Jod. Ein Jodmangel führt zur Verminderung der Hormonproduktion und kann, wie Studien zeigen, die Entstehung einer Hypothyreose begünstigen. Ein anhaltender Mangel kann zudem kardiovaskuläre, knöcherne sowie Verdauungsstörungen verursachen...
Abteilung: Gesundheitsartikel
Kälte, frische Luft und leichter Schnee werden bei den meisten Russen mit Munterkeit, Gesundheit und fröhlichen Aktivitäten assoziiert...
Abteilung: Artikel über Gesundheit
Vitaminkomplexe gehören zu den beliebtesten Präparaten; es gibt keinen Menschen, der nicht von den Vorteilen der Vitamine und deren Mangel gehört hätte. Je mehr Vitamine wir einnehmen, desto besser – doch wie sich zeigte, irren wir uns gewaltig.
Abteilung: Artikel über Gesundheit
Dass eine zuckerreiche Ernährung für die Mehrheit attraktiv ist, ist wissenschaftlich bestätigt. Hier fehlte oft an Disziplin: Die süße Kost vom Säuglingsalter verbindet sich mit dem Gefühl von Ruhe und Sicherheit, das der Kleinstkind beim Absorbieren der Muttermilch erfährt. Zudem verstärkt Zucker im menschlichen Organismus die Wirkung der „Glückshormone", die wir so benötigen. Dennoch findet ein zuckerfreies Leben selten statt: Ihr Verlust ist viel zu groß...
Abteilung: Artikel über Gesundheit