





Klajra
Anwendungshinweise
 Klajra – das kombinierte orale Kontrazeptivum zur Verhinderung einer ungewollten Schwangerschaft.
Klajra – das kombinierte orale Kontrazeptivum zur Verhinderung einer ungewollten Schwangerschaft.
Darreichungsform und Inhalt
Klajra wird als fünf Sorten filmumhüllter Tabletten angeboten: bikonvex, rund; der Querschnitt variiert von fast weiß bis zu weißen Kernfarben sowie dunkelgelb, rosa, blassgelb, rot oder weiß für die Hülle (verpackt in Blister aus Aluminiumfolie/PVC mit 28 Stück; nach einem oder drei Blistern im Buch-Klappbett mit Aufnahmekalender).
Tabletten mit Filmhülle (je Packung 2 Stück): dunkelgelb, auf einer Seite des Sechsecks mit der Aufschrift «DD».
Der Wirkstoff Estradiolvalerat beträgt pro Tablette Mikro-20 bis zu 3 Milligramm.
Filmtabletten (je Packung 5 Stück): rosa, auf einer Seite des Sechsecks mit der Aufschrift «DJ».
Zu jeder Tablette dieses Bestands gehören folgende Wirkstoffe:
- Estradiolvalerat (mikrokristallin) – 2 mg
- Dienogest (mikrokristallin) – 2 mg
Filmtabletten (17 Stück): blassgelb, auf einer Seite im Sechseck mit der Aufschrift «DH»
Zu jeder Tablette dieses Bestands gehören folgende Wirkstoffe:
- Estradiolvalerat (mikrokristallin) – 2 mg
- Dienogest (mikrokristallin) – 3 mg
Filmtabletten (2 Stück): rot, auf einer Seite im Sechseck mit der Aufschrift «DN»
Zu einer Tablette des Bestands gehört der Wirkstoff Estradiolvalerat mikrokristallin – 1 mg
Filmtabletten als Placebos (2 Stück): weiß, auf einer Seite im Sechseck mit der Aufschrift «DT»
Hilfsstoffe (entsprechend den dunkelgelben/rosa/blassgelben/roten/weißen Tabletten): Laktosemonohydrat – 48,36/47,36/46,36/50,36/52,1455 mg; Povidon 25 – 4/4/4/4/3,0545 mg; hydrolysiertes Maisstärkepräparat – 9,6/9,6/9,6/9,6/0 mg; Maisstärke – 14,4/14,4/14,4/14,4/24 mg; Magnesiumstearat – 0,64/0,64/0,64/0,64/0,8 mg
Überzug (entsprechend den dunkelgelben, rosa, blassgelben und roten Tabletten): Hypromellose – 1,5168/1,5168/1,5168/1,0112 mg; Makrogol 6000 – 0,3036/0,3036/0,3036/0 mg; Talkumpulver – 0,3036/0,3036/0,3036/0,2024 mg; Titandioxid – 0,584/0,83694/0,83694/0,5109/0,7864 mg; Eisenoxidgelb – 0,292/0,03906 mg (entsprechend den dunkelgelben und blassgelben Tabletten); Eisenoxidrot – 0,03906/0,3651 mg (entsprechend den rosa und roten Tabletten).
Anwendungshinweise
Klaire zur oralen Empfängnisverhütung anwenden.
Kontraindikationen
- Vorhandensein von Blutgerinnseln und Thrombosen (arteriell oder venös) in der Gegenwart oder in der Vorgeschichte (einschließlich Herzinfarkt, Lungenembolie, tiefe Beinvenenthrombose, Schlaganfall in der Gegenwart oder in der Vorgeschichte);
- Vorhandensein von Risikofaktoren für arterielle oder venöse Thrombosen (einschließlich umfangreiche chirurgische Eingriffe mit längerer Immobilisation, schwerwiegende Herzklappenerkrankungen, unkontrollierte arterielle Hypertonie);
- Vorzeichen einer thrombotischen Erkrankung in der Gegenwart oder in der Vorgeschichte (einschließlich Angina pectoris, ischämische Attacken);
- Diabetes mellitus mit vaskulären Komplikationen;
- Uterine Blutung von ungeklärtem Ursprung.
- Migräne mit herdförmigen neurologischen Symptomen, insbesondere bei Vorliegen in der Anamnese.
- Pankreatitis, die durch eine Hypertriglyceridämie verursacht wird (aktuell oder in der Anamnese).
- Hormonabhängige Malignome, einschließlich Tumore der Brustdrüsen oder der Geschlechtsorgane (bestätigt oder bei Verdacht).
- Bösartige und gutartige Tumore der Leber (aktuell oder in der Anamnese).
- Schwere Lebererkrankungen sowie Pankreasinsuffizienz (die Anwendung von Klajra kann nach Normalisierung der Funktionswerte begonnen werden).
- Schwangerschaft oder der Verdacht auf eine Schwangerschaft
- Überempfindlichkeit gegen die Wirkstoffe des Arzneimittels
Das Präparat darf bei Vorliegen einer der genannten Erkrankungen oder Zustände nicht angewendet werden; falls sich während der Therapie eine dieser Erkrankungen oder Zustände entwickelt, ist die Anwendung von Klajra abzubrechen.
Bei Vorliegen einer der genannten Erkrankungen, Risikofaktoren oder Zustände vor Beginn der Einnahme von Klajra muss das potenzielle Risiko mit dem zu erwartenden Nutzen abgewogen werden (jeder Fall individuell):
- Das erbliche angioneurotische Ödem;
- Arterielle Hypertonie, Rauchen, ausgedehnte Traumata sowie chirurgische Eingriffe, Dyslipoproteinämie, Fettstoffwechselstörungen, Herzrhythmusstörungen, Migräne, Klappenerkrankungen des Herzens, langwierige Immobilisierung und weitere Risikofaktoren für die Entstehung einer Blutpfropfembolie und Thrombose.
- Rote systemisch verlaufende Flechte, Diabetes mellitus, hämolytisch-urämisches Syndrom, granulomatöse Kolitis und ulcerative Kolitis, eisenmangelhafte Anämie sowie weitere Erkrankungen, bei denen Störungen des peripheren Blutkreislaufs beobachtet werden können.
- Erkrankungen, die erstmals während der Schwangerschaft oder im Rahmen einer vorherigen Anwendung von Sexualhormonen auftraten, einschließlich cholestatischer Gelbsucht, Herpes gravidarum, cholestatischem Juckreiz, Chorea gravidatorum, Cholelithiasis sowie Porphyrie mit verstärkter Hörabnahme.
- Hypertriglyceridämie
- Postpartalphase
Anwendungsform und Dosierung
Klaira einnehmen, ggf. mit Wasser oder einem anderen Flüssigkeitsträger, unabhängig von der Nahrungsaufnahme. Das Präparat muss täglich (ununterbrochen) nach einer Tablette pro Tag zu etwa derselben Uhrzeit über einen Zeitraum von 28 Tagen eingenommen werden; danach beginnt die Einnahme aus der neuen Packung.
In der Regel beginnen menstruationsähnliche Blutungen zum Zeitpunkt des Einnehmens der letzten Tabletten der Kalenderpackung. Bei einigen Frauen können sie jedoch bereits nach Beginn der Einnahme aus der neuen Packung einsetzen.
Sollte eine Frau zuvor keine hormonelle Empfängnisverhütung angewendet haben, sollte Klaira am ersten Tag des physiologischen Menstruationszyklus eingenommen werden.
Beim Wechsel von einem anderen kombinierten oralen Kontrazeptivum beginnt die Einnahme von Klaira am nächsten Tag nach dem Einnehmen der letzten Tablette (entsprechend dem Wirkstoffgehalt). Bei Anwendung eines transdermalen Pflasters oder eines vaginalen Rings sollte die Einnahme von Klaira an dem Tag beginnen, an dem das jeweilige Mittel abgetragen wird.
Den Übergang auf den nächsten Tag – entweder durch intramuskuläre Verabreichung des Präparats am Tag der nächsten Injektion oder durch intrauterine Anwendung mit einem Progestagen-Implantat am Tag seiner Entfernung – kann die Therapie fortgesetzt werden. Während der ersten neun Tage nach Beginn der Klaira-Einnahme ist es ratsam, eine zusätzliche Barrieremethode der Kontrazeption anzuwenden.
Nach einem Abort im ersten Schwangerschaftsdrittel kann die Einnahme von Klaira sofort ohne zusätzliche Kontrazeptionsmaßnahmen erfolgen.
Nach einem Abort im zweiten oder dritten Schwangerschaftsdrittel sowie nach der Geburt sollte das Präparat ab dem 21. bis 28. Tag aufgenommen werden. Wurde die Einnahme später begonnen, ist es erforderlich, während der ersten neun Tage eine zusätzliche Barrieremethode zur Kontrazeption anzuwenden. Bei bereits vorhandenem sexuellen Kontakt vor Therapiebeginn muss entweder ein Schwangerschaftsausschluss oder das Eintreten der ersten Menstruation abgewartet werden.
Werden weiße Tabletten versehentlich übersehen, können diese vernachlässigt werden. Solange innerhalb von 12 Stunden keine weiteren Tabletten eingenommen wurden, bleibt der Schutz erhalten; die übersehene Tablette muss dann sofort nachverabreicht werden, sobald sich die Frau daran erinnert. Anschließend wird die Einnahme von Klaira gemäß dem üblichen Schema fortgesetzt.
Wird die Einnahme einer weißen Tablette um mehr als 12 Stunden verzögert, kann der Schutz beeinträchtigt sein. Die übersehene Tablette muss sofort nachverabreicht werden – selbst wenn dies bedeutet, dass zwei Tabletten gleichzeitig eingenommen werden müssen. Anschließend wird die Einnahme von Klaira gemäß dem üblichen Schema fortgesetzt.
Je nachdem, an welchem Tag der Frau eine Tablette übersehen wurde und ob dieser Zeitraum mehr als 12 Stunden beträgt, gelten folgende Regeln:
- Tage 1 bis 2 (Tabletten in dunkelgelber Farbe): Die übersehene Tablette muss sofort nachverabreicht werden. Anschließend wird die Einnahme gemäß dem üblichen Schema fortgesetzt – auch wenn dies bedeutet, dass zwei Tabletten an einem Tag eingenommen werden müssen.
- Tage 3 bis 7 (Tabletten in rosa Farbe): Während dieser neun Tage ist eine zusätzliche Verhütungsmethode erforderlich. Anschließend wird die Einnahme wieder nach dem üblichen Schema fortgesetzt.
- Tage 8 bis 17 (Tabletten in hellgelber Farbe): Während dieser neun Tage ist eine zusätzliche Verhütungsmethode erforderlich.
- Tage 18 bis 24 (Tabletten in hellgelber Farbe): Es muss sofort mit der Einnahme aus einer neuen Packung begonnen werden (ab der ersten Tablette). Während dieser neun Tage ist eine zusätzliche Verhütungsmethode erforderlich.
- Tag 25 und 26 (Tablette in roter Farbe): Die übersehene Tablette muss unverzüglich eingenommen werden. Anschließend erfolgt die Einnahme zur gewohnten Tageszeit, auch wenn an diesem Tag zwei Tabletten eingenommen werden müssen.
- 27. bis 28. Tag (Tablette in weißer Farbe – das Placebo): Die Einnahme von Klajra wird danach wieder nach dem üblichen Schema fortgesetzt; die übersehene Tablette wird nicht eingenommen.
An einem Tag ist es erlaubt, nicht mehr als zwei Tabletten einzunehmen.
Wenn mehrere Tabletten übersehen wurden (in diesem Zeitraum waren zwei Tabletten vom 2. bis zum 24. Tag übersehen), insbesondere bei der Kombination von zwei wirksamen Komponenten, steigt das Risiko einer Schwangerschaft je näher die Phase der Einnahme der inaktiven Tabletten liegt (bei Fällen, in denen im Laufe von sieben Tagen vor dem Ausweis der Tablette sexueller Kontakt bestand).
Bei Abwesenheit mensträhnlicher Blutungen am Ende des laufenden oder Anfang des neuen Zyklus muss die Wahrscheinlichkeit einer Schwangerschaft berücksichtigt werden.
Die Resorption der Wirkstoffe kann bei schweren Magen-Darm-Störungen unvollständig sein; daher ist es empfehlenswert, zusätzliche Verhütungsmaßnahmen anzuwenden.
Für Fälle, in denen sich innerhalb von 3 bis 4 Stunden nach der Einnahme der Tablette mit dem Inhalt des Wirkstoffs Erbrechen entwickelt, gelten die Empfehlungen für übersehene Tabletten. Wenn die Frau das übliche Schema der Einnahme von Klajra nicht einhalten möchte, muss eine entsprechende zusätzliche Tablette aus der neuen Packung eingenommen werden.
Klajra darf Frauen nach dem Einsetzen der Menopause nicht verabreicht werden.
Nebenwirkungen
Bei der Anwendung von Klajra können folgende Nebenwirkungen auftreten:
- Nervensystem: Häufig – Kopfschmerzen (einschl. Anstrengungskopfschmerz); selten – Schwindel, Stimmungstiefs/Depression, Libidoverlust, psychische Störungen, Stimmungsschwankungen; selten – Aggressivität, Affektlabilität, Nervosität, Angstzustände, Libidozunahme, Aufmerksamkeitsstörungen, Verstimmung, Traumstörungen, Stress, Unruhe, Vertigo, Paresthesien.
- Verdauungssystem: Häufig – Bauchschmerzen (einschließlich Blähungen); selten – Übelkeit, Durchfall, Erbrechen; selten – gastroösophageale Refluxkrankheit.
- Kardiovaskuläres System: Selten – arterielle Hypertonie, Migräne (mit und ohne Aura); selten – Hitzewallungen, Blutungen aus Krampfadern, Schmerzen in den Venen, arterielle Hypotonie.
- Sexuelles System: Häufig – Dyskomfort und Schmerzen in den Brustdrüsen, Amenorrhö, Verletzungen der Brustwarzen, Dysmenorrhöe, Schmerzen in den Brustwarzen, Menorrhagie; Selten – Zunahme und diffuse Induration der Brustdrüsen, fibrozystische Mastopathie, Epitheldysplasie des Gebärmutterhalses, Dyspareunie, Funktionsstörungen der Eierstöcke mit Blutungen, Menorrhagie, Schmerzen im Schamlippenbereich, Ovarialzysten, prämenstruelles Syndrom, Leiomyom uteri, vaginale Sekrete, Krämpfe in der Gebärmutter, Trockenheit im Scheiden- und vaginalen Bereich; Selten – gutartige Neubildungen in der Brustdrüse, Galaktorrhoe, Zyste der Brustdrüse, Blutung während des Geschlechtsverkehrs, Blutung aus der Scheide, Unterbrechung menstruationsähnlicher Blutungen, Hypomenorrhöe, Ruptur einer Ovarialzyste, Brennen im Scheidenbereich, vaginale Dyskomfort/Scheidenblutung (mit vaginalem Unwohlsein, Geruch und Schleimabsonderung).
- Leber: Selten – fokale Leberhyperplasie, erhöhte Alaninaminotransferase-Aktivität.
- Knochen- und Muskelsystem: Selten – Schweregefühl, Muskelkrämpfe, Rückenschmerzen.
- Subkutanes Gewebe und Haut: Häufig – Akne. Selten – Alopezie, Ausschlag (einschließlich fleckiger Ausschläge), Juckreiz (mit juckendem Ausschlag oder generalisiertem Juckreiz); selten – Neurodermitis, allergische kutane Reaktionen (einschließlich Urtikaria und allergischer Dermatitis), Dermatitis, Chloasma, Hirsutismus, Hypertrichose, Seborrhoe, Pigmentstörungen sowie unpräzisierte Hautinfektionen mit Spannungsgefühl der Haut.
- Sehorgan: Selten – Intoleranz gegenüber Kontaktlinsen.
- Invasionen und Infektionen: Selten – Pilzinfektionen, Candidose der Scheide sowie unpräzisierte Scheideninfektionen; selten – vaginale Pilzinfektionen, Trichomoniasis, Herpes, vermutete Histoplasmose des Auges, bakterielle Vaginose sowie Harnwegsinfekte.
- Ernährungsstörungen und Stoffwechsel: Selten gesteigerte Appetitneigung; selten Hypertriglyceridämie sowie Flüssigkeitsretention.
- Allgemeine Symptome: Häufig eine Zunahme der Körpermasse. Selten Abnahme der Körpermasse, Ödeme, Reizbarkeit, Unwohlsein, Schmerzen hinter dem Brustbein, Lymphadenopathie und Erschöpfung.
Besondere Hinweise
Vor Beginn der Anwendung von Klajra ist es notwendig, die Kontraindikationen sorgfältig zu bewerten, basierend auf der Familienanamnese der Frau, ihrer Krankengeschichte sowie gynäkologischen und allgemeinen medizinischen Untersuchungen.
Das höchste Risiko für das Auftreten einer Venenthrombose liegt im ersten Jahr nach Beginn der Einnahme von Klajra (vorzugsweise in den ersten drei Monaten).
Eine Thrombose anderer Blutgefäße – beispielsweise der Mesenterialvene, Lebervene, Nierenvene sowie der Hirnvenen und -adern – entwickelt sich äußerst selten.
Das Risiko für das Auftreten einer Embolie und Thrombose (arteriell und/oder venös) nimmt bei Rauchern mit zunehmendem Alter sowie bei Vorliegen der folgenden Erkrankungen oder Zustände zu:
- Ein Hinweis auf eine Venen- oder Arterienembolie in der Familienanamnese;
- Stoffwechselstörungen des Fettstoffwechsels (bei einem Body-Mass-Index von mindestens 30 kg/m²);
- Vorhofflimmern;
- Lipidstoffwechselstörungen (bei einem Body-Mass-Index von mindestens 30 kg/m²);
- Arterielle Hypertonie;
- Herzklappenerkrankungen
- Migräne
- Langzeitimmobilisation
- Umfassende chirurgische Eingriffe, insbesondere Operationen an den unteren Extremitäten sowie schwere Traumata.
Das erhöhte Risiko einer Thromboembolie in der nachfolgenden Phase muss berücksichtigt werden. Zudem ist die Entwicklung von Störungen des peripheren Blutkreislaufs bei Frauen mit Diabetes mellitus, Lichen ruber planus, hämolytisch-urämischem Syndrom sowie bei langdauernden entzündlichen Darmerkrankungen (Granulomatöse Kolitis oder Ulzerative Kolitis) und bei Eisenmangelanämie möglich.
Eine Zunahme der Schwere und Häufigkeit der Migräne kann als Indikation für die sofortige Einstellung der Klajra-Therapie dienen.
In seltenen Fällen der Anwendung des Präparats entwickelten sich gutartige Tumoren, in äußerst seltenen Fällen Lebermalignome. Bei Auftreten starker Schmerzen im Oberbauch, bei Vergrößerungen der Leber oder Symptomen einer intraabdominalen Blutung ist im Rahmen der Differentialdiagnostik die Ausschlussdiagnose von Lebertumoren erforderlich.
Das Risiko einer Pankreatitis ist bei Frauen mit Hypertriglyceridämie erhöht.
Die Klajra-Therapie muss bei anhaltender, klinisch relevanter arterieller Hypertonie abgebrochen werden.
Bei erblichen Formen des angioneurotischen Ödems kann das Präparat die Symptome verschlimmern.
Die Einnahme von Klajra kann die Ergebnisse laborchemischer Untersuchungen beeinflussen, einschließlich biochemischer Kennwerte der Schilddrüse, Leber-, Nieren- und Nebennierenfunktion sowie der Konzentration der Transportproteine im Plasma; zudem können sich Werte des Wasserstoffwechsels, der Fibrinolyse und der Blutgerinnung verändern.
Während der Klajra-Therapie, insbesondere in den ersten Monaten, ist das Auftreten unregelmäßiger menstruationsähnlicher Blutungen möglich, die als schmierende oder starke Blutungen beschrieben werden. Die Bewertung solcher Blutungen sollte erst nach mindestens drei Zyklen (nach der Anpassungsphase) erfolgen.
Bei wiederholtem Auftreten unregelmäßiger, menstruationsähnlicher Blutungen – insbesondere wenn diese erstmals nach vorhergehenden regelmäßigen Zyklen entstehen – ist eine sorgfältige Abklärung erforderlich, um bösartige Neubildungen oder eine Schwangerschaft auszuschließen.
Die Wirksamkeit von Klajra kann bei Magen-Darm-Störungen sowie durch die Einnahme von Tabletten mit flüssigem Inhalt oder aufgrund begleitender medikamentöser Therapien verringert werden.
Arzneimittelwechselwirkungen.
Die gleichzeitige Einnahme von Klajra mit bestimmten anderen Arzneimitteln kann zu einem Ausfall der kontraceptiven Wirkung und/oder zum Auftreten starker Blutungen führen. Insbesondere müssen die Effekte der Kombination von Klajra mit den folgenden Präparaten berücksichtigt werden:
- Rifampicin, Carbamazepin, Phenytoin, Primidon, Barbiturate sowie möglicherweise auch Oxcarbazepin, Griseofulvin, Topiramat, Ritonavir und Felbam; zudem Präparate mit einem hohen Gehalt an induzierenden Enzymen: Eine Erhöhung der Clearance von Sexualhormonen.
- Nichtnukleosidische Reverse-Transkriptase-Hemmer (zum Beispiel Nevirapin) sowie Proteasehemmer (zum Beispiel Ritonavir): Einfluss auf die hepatische Metabolisierung.
- Präparate, die mikrosomale Enzyme induzieren, sowie Antibiotika: Sie senken die enterohepatische Zirkulation der Östrogene und führen damit zu einer Verringerung der Estradiolkonzentration (es wird empfohlen, während der Anwendung dieser Präparate sowie noch 28 Tage nach deren Absetzen alternative Kontrazeptionsmethoden oder Barrieremethoden anzuwenden).
- Grapefruitsaft, azolische Antimykotika, Verapamil, Zimetidin, Diltiazem und Makrolide: Sie erhöhen die Konzentration von Dienogest im Blutplasma.
Lagerung und Haltbarkeit
An einem für Kinder unzugänglichen Ort bei Temperaturen von bis zu 30 °C lagern.
Haltbarkeitsdauer: 4 Jahre
Arzneimittelname
Preis
Apotheke
Klajra-Tabletten, 28 Stück
1028 Rubel
Kaufen
 Apotheke der russischen Föderation, Gesellschaft mit beschränkter Haftung
Apotheke der russischen Föderation, Gesellschaft mit beschränkter Haftung
Klajra-Tabletten, 28 Stück, Hersteller: Bayer
1221 Rubel
Kaufen
 Moskauer Apothekennetzwerk IFK
Moskauer Apothekennetzwerk IFK
Klajra-Tabletten, 28 x 3 Stück
2.633 Euro
Kaufen
 Apotheke der russischen Föderation, Gesellschaft mit beschränkter Haftung
Apotheke der russischen Föderation, Gesellschaft mit beschränkter Haftung
Klajra-Tabletten, 84 Stück, Hersteller Bayer
3.147 Euro
Zur Verfügung im Verkauf
 IFK-Apothekennetzwerk Moskau
IFK-Apothekennetzwerk Moskau
Der 74-jährige Australier James Harrison war über 1000 Mal Blutspender. Seine seltene Blutgruppe ermöglicht es, Neugeborene mit schwerer Anämie zu retten. So hat er zwei Millionen Kinder gerettet.

Singen Sie gerne? Während sich kleine Kinder oft mit Gesang beschäftigen, ohne die Melodie besonders zu beachten, sehen Erwachsene dies meist anders.
Rubrik: Artikel zur Gesundheit.
Die Diätologie sowie weitere Wissenschaften sind kostenlos: Lebensmittel werden umfassend untersucht, sodass Gelehrte neue Informationen über ihre Eigenschaften und ihren Einfluss auf den menschlichen Organismus erhalten. Leider wird dieser vernünftige und physiologische Prozess von Zeit zu Zeit unterbrochen...
Rubrik: Artikel zur Gesundheit.
Der Begriff 'Kleber' (alternativ auch als Klebstoff bezeichnet) umfasst die Gruppe der Proteine, die in Roggen, Gerste und Weizen vorkommen. Für die Mehrheit der Menschen ist der Verzehr von Lebensmitteln, die Gluten enthalten, nicht nur sicher, sondern auch sehr nützlich. Dennoch gibt es eine ganze Reihe von Mythen über negative Effekte, die angeblich das Gluten auf die menschliche Gesundheit hat...
Rubrik: Artikel zur Gesundheit.
Bei allen Nervenkrankheiten – in diesem Witz steckt ein großer Kern der Wahrheit, sagen die Ärzte: Ständiger Stress führt zu einer Schwächung des Immunsystems...
Rubrik: Artikel zur Gesundheit.
Oft dient unsere Wohnung als Infektionsquelle und verursacht Erkrankungen; sie soll eigentlich sicher sein. Jedoch können krankheitserregende Bakterien sich nicht nur in unhygienischen Bedingungen, sondern auch in unserer Wohnung wohlfühlen, wenn diese nicht ausreichend sauber ist...
Abteilung: Artikel zur Gesundheit
Die Depression wird nicht umsonst zu einer Hauptnot unseres Jahrhunderts gerechnet: Für den wissenschaftlich-technischen Fortschritt, die Beschleunigung des Lebenstempos und das Informationsübermaß ist der Mensch gezwungen, Stress, negative Emotionen und die Schwächung der Abwehrkräfte des Organismus zu erleiden. Infolgedessen manifestieren sich Zustände, die durch erhöhte Angst gekennzeichnet sind, den Verlust des Interesses am Leben sowie geistige und körperliche Dyskomfortzustände.
Abteilung: Artikel zur Gesundheit
Musiktherapie ist eine Behandlungsweise, deren Effektivität kontrovers diskutiert wird; die Ergebnisse sind jedoch eindeutig:
Abteilung: Artikel zur Gesundheit
In modernen Geschäften findet man ein umfangreiches Sortiment an Früchten und Gemüse. Die Russen haben sich daran gewöhnt: Auf den Ladentischen finden sich nicht nur die einheimische Saisonproduktion, sondern auch Gemüse und Früchte aus Ländern mit günstigeren Bedingungen, die das ganze Jahr über verfügbar sind.
Abteilung: Artikel zur Gesundheit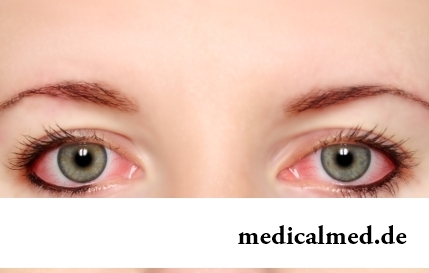
Sklera und Bindehaut des Auges werden durch Blutgefäße versorgt, deren Aufgabe es ist, das nervöse Gewebe des Organs intensiv mit Nährstoffen und Sauerstoff zu sättigen. Im Normalzustand sind diese Gefäße kaum sichtbar; jedoch führen bei ihrer Erweiterung (infolge der Wandverdickung) die Sklera zur Rotfärbung. Nicht selten rote Augen – ein Signal für verschiedene Störungen im Organismus, bedingt durch exterozeptive Reize, Allergene sowie Krankheiten, die einen erhöhten Sauerstoffbedarf verursachen.
Abteilung: Artikel zur Gesundheit
In der Medizin werden Infektionen, die vorwiegend über den sexuellen Weg übertragen werden, als Geschlechtskrankheiten bezeichnet; derzeit sind sie wie folgt...
Die Abteilung: Artikel über Gesundheit
Ein gesundes und gepflegtes Aussehen bedeutet nicht nur, der Umgebung zu gefallen, sondern auch, sich stark, überzeugt und vital zu fühlen. Experten auf dem Gebiet der Kosmetologie betonen häufig, dass die meisten Frauen verstehen, wie wichtig es ist, für die Haut zu sorgen.
Die Abteilung: Artikel über Gesundheit
Olivenöl leistet einen wichtigen Beitrag zur menschlichen Gesundheit, wenn man es in die Ernährung aufnimmt. Der hohe Vitamingehalt macht dieses Öl zu einem der wichtigsten Mittel gegen viele Krankheiten, einschließlich tödlicher Erkrankungen. Bereits zwei Esslöffel Olivenöl können das Auftreten von Erkrankungen wie Darmproblemen und Herzkrankheiten sowie vorzeitiges Altern, Depressionen und andere Leiden verhindern, deren Behandlung sonst viel Zeit und Kraft erfordert hätte.
Die Abteilung: Artikel über Gesundheit
Keiner von uns ist gegen schweres Leid naher Menschen versichert. Es kommt daher vor, dass ein Familienmitglied an Krebs erkrankt.
Die Abteilung: Artikel über Gesundheit
Das endokrine System erfüllt im menschlichen Organismus eine außerordentlich wichtige Rolle; praktisch alle Prozesse des Lebensverlaufs werden durch es reguliert. Die Drüsen produzieren spezielle Wirkstoffe – die Hormone –, die dann biologisch aktiv sind.
Die Abteilung: Artikel über Gesundheit
Eine Erkältung ist ein jedem bekannter Zustand, der durch Schnupfen, Husten, hohes Fieber und Halsbeschwerden begleitet wird. Oft beginnen wir zunächst mit Medikamenten in der Hoffnung, schnell wieder gesund zu werden; diese Mittel sind jedoch nicht immer unschädlich. Es ist viel einfacher, die Krankheitserscheinungen mit Hilfe natürlicher Mittel zu lindern. Sie entfernen nicht nur die Symptome, sondern bereichern auch den geschwächten Organismus mit nützlichen Substanzen. Wir stellen Ihnen 8 Getränke vor, die erfolgreich eingesetzt werden können...
Die Abteilung: Artikel über die Gesundheit
Die Heckenrose – eine der am weitesten verbreiteten dekorativen und Arzneipflanzen, die tatsächlich auf dem gesamten Territorium unseres Landes wächst...
Die Abteilung: Artikel über die Gesundheit
Unter einer Vielzahl parfüm-kosmetischer Waren, die heute angeboten werden, bilden Mittel mit antibakteriellen Komponenten eine besondere Gruppe. Solche Produkte wie Gele, Shampoos, Seifen, Cremes, Lotionen und andere werden von den Herstellern als Allheilmittel positioniert...
Die Abteilung: Artikel über die Gesundheit
Für den Stadtbewohner ist das Fitnessstudio die bequemste Sportart. Es genügt, ein Abonnement für die Sporthalle zu erwerben, um Zugang zu vielfältigen Sportgeräten und die Möglichkeit zu erhalten, unter Anleitung eines erfahrenen Trainers zu trainieren. Viele halten das Fitnessstudio für die beste Methode zur Aufrechterhaltung der körperlichen Form und zum Erhalt der dynamischen Belastungen, die insbesondere Menschen benötigen, die vorwiegend geistige Arbeit leisten. Dennoch ist die Vorstellung der Mehrheit der Konsumenten ähnlicher Dienstleistungen über spezifische...
Die Abteilung: Artikel über die Gesundheit
Die Fettleibigkeit wird seit dem 21. Jahrhundert als Krankheit bezeichnet; in den letzten 100 Jahren ist die Anzahl der Menschen, die an Übergewicht leiden, erheblich gestiegen...
Die Abteilung: Artikel über die Gesundheit
Der Arztbesuch ist nicht immer angenehm, und viele beeilen sich nicht, die notwendigen regelmäßigen Untersuchungen wahrzunehmen. Solches Verhalten erscheint leichtfertig und nachlässig. Doch unsere Gesundheit ist nicht nur uns selbst notwendig: das Wohlergehen der Partner, Kinder, Enkel und anderer...
Abteilung: Artikel zur Gesundheit
In der Geschichte der Menschheit wurden Dutzende Epidemien registriert, deren Ausbruch von Zeitzeugen und Historikern oft als das Ende des Lichtes beschrieben wurde. Die verheerendsten davon haben Millionen Leben gerafft und ganze Völker vernichtet. Welche Krankheiten verursachen den Schrecken? Ist es dem Menschen gelungen, eine Behandlung zu finden, oder bleibt er vor den Kräften der Natur ohnmächtig?
Abteilung: Artikel zur Gesundheit
Die Nieren erfüllen die wichtigste Funktion der Blutreinigung von Stoffwechselprodukten, die vom Körper nicht verwertet werden können.
Abteilung: Artikel zur Gesundheit
Zu den nützlichen Eigenschaften, die dem Menschen von der Natur geschenkt wurden, zählt die Fähigkeit, Angst auszustehen. Gerade diese Fähigkeit dient dazu, eine gefährliche Situation zu signalisieren und im Voraus das Leben zu retten. Jedoch ist dies nur dann vorteilhaft, wenn die Angst nicht übertrieben ist...
Abteilung: Artikel zur Gesundheit
Das Befinden des Menschen hängt von vielen Faktoren ab. Eine der wichtigsten ist ständig vorhanden, ohne jedoch schädlich zu sein: die Bewegungsaktivität. Bei verschiedenen Leiden beraten Experten Patienten oft dazu, sich mit Seefahrt zu beschäftigen, was nachweislich eine hohe Heilungseffektivität aufweist und nur wenige Kontraindikationen hat. Heute werden wir über die Hauptrichtungen der therapeutischen Wirkung von Seefahrt auf den menschlichen Organismus sprechen.
Abteilung: Artikel zur Gesundheit
Die Mehrzahl der gynäkologischen Erkrankungen manifestiert sich durch drei Hauptmerkmale; jedes dieser Merkmale weist auf eine bestimmte Notwendigkeit hin...
Abteilung: Artikel über Gesundheit
Auf dem menschlichen Kopf befinden sich neben Millionen Haarfollikel, die auch als Haarzwiebeln bezeichnet werden. Zum Zeitpunkt der Geburt befindet sich die Mehrzahl dieser Follikel in einem ‚schlafenden' Zustand, wird jedoch im Laufe einiger Wochen aktiviert und beginnt...
Abteilung: Artikel über Gesundheit
Zu den Stereotypen, über die allgemein bekannt ist, gehört folgendes feststehendes Urteil: Die Engländer essen zum Frühstück zwingend Haferbrei. Zwar trifft dies auf viele moderne Bewohner Britanniens zu; dennoch kann man aufrichtig erfreut sein, dass sie dieser Tradition weiterhin folgen. Haferflocken sind ein Produkt, dessen regelmäßige Anwendung dem Menschen langfristig Kraft und Schönheit erhält. Der Haferbrei wirkt auf den Organismus in besonderer Weise schützend...
Abteilung: Artikel über Gesundheit
